Повідомлення Державної служби з лікарських засобів та контролю за наркотиками у Хмельницькій області від 31.03.2023 №43-01.1/02-30/05.23-23
Опубліковано 03.04.2023 о 09:43
ДЕРЖАВНА СЛУЖБА УКРАЇНИ З ЛІКАРСЬКИХ ЗАСОБІВ
ТА КОНТРОЛЮ ЗА НАРКОТИКАМИ
ДЕРЖАВНА СЛУЖБА З ЛІКАРСЬКИХ ЗАСОБІВ ТА КОНТРОЛЮ
ЗА НАРКОТИКАМИ У ХМЕЛЬНИЦЬКІЙ ОБЛАСТІ
Львівське шосе, 12, м. Хмельницький, 29016, тел/факс: (0382) 72-32-13, 66-01-07, 72-32-02
е-mail: dls.km@dls.gov.ua, Код ЄДРПОУ 37098188
|
“31” 03 2023р. №43-01.1/02-30/05.23-23 |
Керівникам суб’єктів господарювання, лікувально-профілактичних закладів, які займаються реалізацією (торгівлею), зберіганням та медичним застосуванням лікарських засобів (за списком) |
ПОВІДОМЛЕННЯ
1. ФАЛЬСИФІКАЦІЯ
1.1. На підставі інформації Представництва Елі Ліллі Восток С.А. (Швейцарія) в Україні, що представляє інтереси власника реєстраційного посвідчення Елі Ліллі Недерленд Б.В. (листи від 13.03.2023 №5038, від 28.03.2023 №5043) щодо виявлення в обігу на території України фальсифікованих серій 1128535А, 1130718А лікарського засобу іноземною мовою, які за інформацією представництва ніколи не вироблялись та не випускались компанією Ліллі, з метою активної протидії поширенню фальсифікованих лікарських засобів, що можуть спричинити розвиток хвороби або неналежне лікування, нести потенційну загрозу життю та здоров’ю населення і є небезпечним – забороняється реалізація, зберігання та застосування фальсифікованого лікарського засобу:
– СІАЛІС, серій 1128535А, 1130718А, з маркуванням виробника Ліллі, іноземною мовою.
/Розпорядження Держлікслужби №2945-001.1/002.0/17-23 від 30.03.2023/.
1.2. На підставі інформації ТОВ “Ново Нордікс Україна”, що діє від імені власника реєстраційного посвідчення А/Т Ново Нордіск, Данія (листи від 24.03.2023 №109, від 29.03.2023 №116) щодо виявлення в обігу на території України лікарських засобів, які є фальсифікованими, та мають наступні ознаки фальсифікації (Додаток 1) від оригінальних препаратів. З метою активної протидії поширенню фальсифікованих лікарських засобів, що можуть спричинити розвиток хвороби або неналежне лікування, нести потенційну загрозу життю та здоров’ю населення і є небезпечним – забороняється реалізація, зберігання та застосування фальсифікованих лікарських засобів:
– ОЗЕМПІК, розчин для ін’єкцій, 1,34мг/мл; 0,25мг: по 1,5мл у картриджах, вкладених у попередньо заповнену багатодозову одноразову шприц-ручку; 1 попередньо заповнена шприц-ручка та 6 одноразових голок НовоФайн® Плюс в картонній коробці, серії MP5B060, та
ОЗЕМПІК, розчин для ін’єкцій, 1,34мг/мл; 1мг: по 3мл у картриджах, вкладених у попередньо заповнену багатодозову одноразову шприц-ручку; 1 попередньо заповнена шприц-ручка та 4 одноразових голки НовоФайн® Плюс в картонній коробці, серії МР5В060, з маркуванням виробництва А/Т Ново Нордіск, Данiя, англійською мовою, з ознаками фальсифікації (Додаток 1).
/Розпорядження Держлікслужби №2943-001.1/002.0/17-23 від 30.03.2023/.
При виявленні зразків вказаних лікарських засобів вжити заходи щодо вилучення їх з обігу шляхом розміщення в карантин.
2. ЗАБОРОНЯЄТЬСЯ
2.1. На підставі інформації власника реєстраційного посвідчення ТОВ “Бауш Хелс” від 21.03.2023 №5 щодо невідповідності лікарського засобу, вимогам МКЯ до реєстраційного посвідчення №UA/5204/01/01 за показником “Хроматографічна чистота: – будь-якої невідомої домішки” (за результатами дослідження стабільності) – забороняється реалізація, зберігання та застосування лікарського засобу:
– ОМНАДРЕН® 250, розчин олійний для ін’єкцій, по 1 мл у ампулі, по 5 ампул у картонній коробці, серії 204021, виробництва Фармзавод “Єльфа” A.Т., Польща (реєстраційне посвідчення №UA/5204/01/01).
/Розпорядження Держлікслужби №2714-001.1/002.0/17-23 від 24.03.2023/.
2.2. На підставі повідомлення імпортера лікарського засобу ТОВ Конарк Інтелмед від 23.03.2023 №321/B щодо відклику виробником Індоко Ремедіс Лімітед, Індія, з обігу на території України лікарського засобу, серій 22010461, 22010462, 22010463 (реєстраційного посвідчення №UA/2515/01/01), щодо невідповідності за показником “Мікробіологічна чистота” – забороняється реалізація, зберігання та застосування лікарського засобу:
– КАЛЬЦИКЕР, суспензія оральна по 120мл у флаконі; по 1 флакону разом з мірною ложкою у картонній упаковці, серій 22010461, 22010462, 22010463, виробництва Індоко Ремедіс Лімітед, Індія (реєстраційне посвідчення №UA/2515/01/01).
/Розпорядження Держлікслужби №2941-001.1/002.0/17-23 від 30.03.2023/.
2.3. На підставі повідомлення виробника ТОВ “Фармацевтична компанія “Здоров’я”, Україна, щодо відклику з обігу на території України лікарського засобу серії 21022, у зв’язку з виявленою невідповідністю щодо умов його зберігання – забороняється реалізація, зберігання та застосування лікарського засобу:
– ТОЛПЕРІЛ-ЗДОРОВ’Я, розчин для ін’єкцій, по 1мл в ампулі; по 5 ампул у картонній коробці з перегородкою; по 5 ампул у блістері; по 1 блістеру у коробці з картону, серії 21022, виробництва ТОВ “Фармацевтична компанія “Здоров’я”, Україна (реєстраційне посвідчення №UA/19576/01/01).
/Розпорядження Держлікслужби №2944-001.1/002.0/17-23 від 30.03.2023/.
При виявленні зразків вказаних лікарських засобів вжити заходи щодо вилучення їх з обігу шляхом повернення постачальнику/виробнику або знищення.
3. НЕЗАРЕЄСТРОВАНІ
3.1. На підставі інформації Служби безпеки України від 22.03.2023 від 5/7/4/4-7768 щодо обігу незареєстрованих лікарських засобів з маркуванням іноземною мовою та з метою активної протидії поширенню незареєстрованих лікарських засобів, що офіційно не ввозились на територію України, є небезпечними та можуть спричинити розвиток хвороби або неналежне лікування, нести потенційну загрозу життю та здоров’ю населення – забороняється реалізація, зберігання та застосування всіх серій незареєстрованих лікарських засобів з маркуванням іноземною мовою:
|
Назва та форма лікарського засобу |
Виробник |
|
BLEOMEDAC, 15000 IU |
Medac Gesselschaft (Germany) |
|
FEMODENE |
Schering GmbH & Co. Productions KG |
|
FOSINOPRIL, 20mg tablet |
Rivopharm Limited |
|
GYNATREN |
Strathmann GmbH & Co.KG (Germany) |
|
LESCOL XL, 80mg |
Novartis (Угорщина) |
|
MIRVASO, 3mg/g gel |
Galderma |
|
OSPOLOT, 20mg/ml |
Desitin Arzneimittel GmbH (DEU) |
|
PRESTARIUM COMBI A |
Les Laboratoires Servier |
|
TETMODIS, 25mg |
AOP Orphan Pharmaceuticals AG (Австрія) |
|
UNITROPIC, 0,5% |
Unimed Pharma |
/Розпорядження Держлікслужби №2758-001.1/002.0/17-23 від 27.03.2023/.
При виявленні зразків вказаних лікарських засобів, вжити заходи щодо вилучення їх з обігу шляхом знищення.
При наступних поставках вжити заходи щодо запобігання придбанню, застосуванню та реалізації лікарських засобів, наведених в повідомленні.
Результати опрацювання повідомлення надати письмово до Державної служби з лікарських засобів та контролю за наркотиками у Хмельницькій області (29016 м. Хмельницький, Львівське шосе,12) до 07.04.2023р. з відповідними документами.
Відповідальність за виконання розпоряджень покладається на керівників суб’єктів господарювання.
Невиконання розпорядження Державної служби тягне за собою відповідальність згідно з чинним законодавством України.
Начальник служби Ігор МІЛІНЧУК
Ставицька Наталія 72-32-02
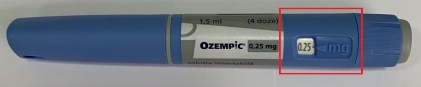
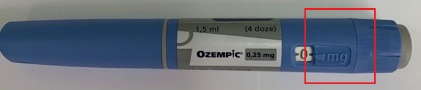
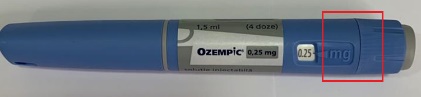
Ознаки фальсифікації шприц-ручки (первинної упаковки) Додаток 1
лікарського засобу Ozempic®
|
Опис |
Оригінальний ЛЗ |
Фальсифікований ЛЗ |
Оригінальні частини шприц-ручки та голки |
Фото оригінального ЛЗ |
Фото фальсифікованого ЛЗ |
|
|
1 |
Загальне фото шприц-ручки ЛЗ Ozempic® |
—- |
—- |
—– |
|
|
|
2 |
Наявність одноразових голок НовоФайн® Плюс в картонній коробці |
0,25/0,5 мг: по 1,5мл 6 одноразових голок НовоФайн® Плюс |
Відсутні взагалі або може містити недостатню кількість |
|
—— |
—— |
|
1 мг: по 3мл 4 одноразових голки НовоФайн® Плюс |
Відсутні взагалі або може містити недостатню кількість |
|||||
|
3 |
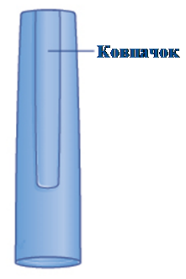
Наявність логотипу на ковпачку первинної упаковки (шприц-ручки) |
Наявний |
Відсутній |
|
|
|
|
4 |
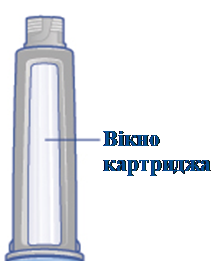
Картридж та вікно картриджа (розмір, колір та дизайн) |
0,25/0,5мг: по 1,5мл Розмір картриджа: 3,3см Колір картриджа: сірий Колір вікна картриджа: прозорий |
Розмір картриджа: Однаковий Колір картриджа: прозорий Колір вікна картриджа: вікно відсутнє |
|
|
|
|
1мг: по 3мл Розмір картриджа: 5,5см Колір картриджа: сірий Колір вікна картриджа: прозорий |
||||||
|
5 |
Розміщення етикетки до лічильника дози |
Близько |
Далеко |
|
|
|
|
6 |
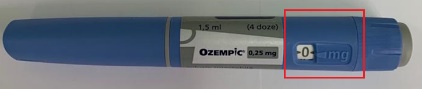
При повертанні селектора дози вперед, щоб обрати дозу, лічильник дози покаже відповідну дозу |
0,25/0,5мг: по 1,5мл 0мг; 0,25мг/ 0мг; 0,5мг |
Від 0 до 80 |
|
|
|
|
1 мг: по 3мл 0мг, 1мг |
||||||
|
7 |
При повертанні селектора дози вперед, щоб обрати дозу |
Шприц-ручка не змінюється в довжині |
Шприц-ручка змінюється в довжині (вона постійно зміщується (збільшується)) |
|
|
|
|
8 |
Наявність покажчика дози |
Наявний |
Відсутній |
|
|
|
|
9 |
Колір пускової кнопки |
Сірий |
Фіолетовий |
|
|
|
|
10 |
Наявність в лічильнику дози символу перевірки потоку розчину ( |
Наявний |
Відсутній |
|
—– |
|
 Людям із порушенням зору
Людям із порушенням зору  In English
In English 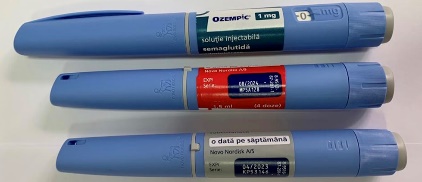





























 Попередня
Попередня