Процес проходження процедури підтвердження відповідності умов виробництва лікарських засобів
Опубліковано 06.12.2024 о 14:37![]() 05 грудня 2024 року Державна служба України з лікарських засобів та контролю за наркотиками запускає бета-версію дашборду процесу проходження процедури підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP).
05 грудня 2024 року Державна служба України з лікарських засобів та контролю за наркотиками запускає бета-версію дашборду процесу проходження процедури підтвердження відповідності умов виробництва лікарських засобів вимогам належної виробничої практики (GMP).
![]() Дає можливість:
Дає можливість:
∙ відстежити стан розгляду заяв на відповідність вимогам GMP
∙ оперативно отримати інформацію щодо прийнятих рішень.
![]() Як скористатися?
Як скористатися?
1. Перейдіть за посиланням:
![]() https://gmp.dls.gov.ua
https://gmp.dls.gov.ua
2. Введіть логін та пароль, що ви отримали на вашу електронну пошту після реєстрації заяви.
3. Перегляньте стан розгляду вашої заяви.
![]() Звертаємо вашу увагу, що дашборд міститиме дані щодо статусу заяв зареєстрованих з 05 грудня 2024 року.
Звертаємо вашу увагу, що дашборд міститиме дані щодо статусу заяв зареєстрованих з 05 грудня 2024 року.
![]() Інструмент працює у бета-версії (режимі тестування).
Інструмент працює у бета-версії (режимі тестування).
![]() У разі виявлення помилок або невідповідностей, прохання повідомити нам за адресою: GMP@dls.gov.ua
У разі виявлення помилок або невідповідностей, прохання повідомити нам за адресою: GMP@dls.gov.ua
Дякуємо за співпрацю!
 Людям із порушенням зору
Людям із порушенням зору  In English
In English 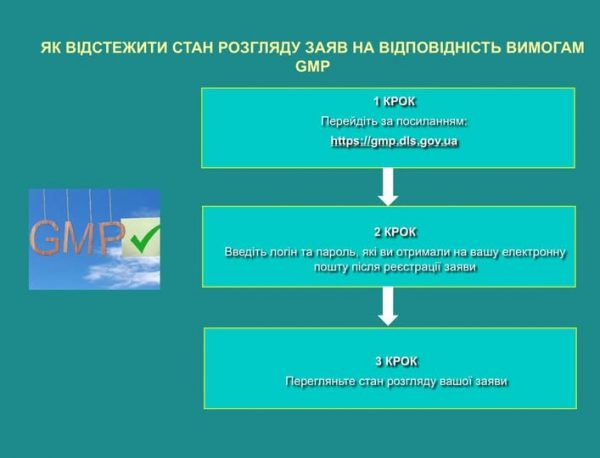

 Попередня
Попередня